สารในชีวิตประจำวันเช่นแก๊สออกซิเจน (O₂) และแก๊สคาร์บอนไดออกไซด์ (CO₂) ที่เกี่ยวข้องกับกระบวนการหายใจของสิ่งมีชีวิต น้ำ (H₂O) เป็นของเหลวที่ใช้ในการอุปโภคและบริโภค เกลือแกง (NaCl) เป็นของแข็งที่ใช้ในการประกอบอาหาร สารเหล่านี้ส่วนใหญ่ไม่อยู่ในรูปอะตอมเดี่ยวแต่ประกอบด้วยหลายอะตอม ซึ่งอาจเป็นอะตอมชนิดเดียวกันหรือต่างชนิดกัน การยึดเหนี่ยวกันของอะตอมหรือไอออนในสารเรียกว่าพันธะเคมี (chemical bond)
3.1 สัญลักษณ์แบบจุดของลิวอิสและกฎออกเตต
จากการศึกษาเรื่องอะตอมและสมบัติของธาตุทำให้ทราบว่า เวเลนซ์อิเล็กตรอนเป็นอิเล็กตรอนที่อยู่ในระดับพลังงานสูงสุดหรือชั้นนอกสุดของอะตอม เช่น ธาตุคาร์บอนมีการจัดเรียงอิเล็กตรอนในระดับพลังงานย่อยเป็น 1s² 2s² 2p² ดังนั้น คาร์บอนมีเวเลนซ์อิเล็กตรอนเท่ากับ 4 ทั้งนี้การเกิดพันธะเคมีเกี่ยวข้องกับเวเลนซ์อิเล็กตรอนของคู่อะตอมที่ร่วมสร้างพันธะกัน
เวเลนซ์อิเล็กตรอนของธาตุอาจแสดงด้วยจุดสัญลักษณ์ที่แสดงธาตุและเวเลนซ์อิเล็กตรอนของธาตุเรียกว่า สัญลักษณ์แบบจุดของลิวอิส (lewis dot symbol) ซึ่งเสนอโดย กิลเบิร์ต นิวตัน ลิวอิส
สัญลักษณ์แบบจุดของลิวอิสใช้จุดแสดงจำนวนเวเลนซ์อิเล็กตรอนรอบสัญลักษณ์ของธาตุดังรูป โดยเขียนจุดเดี่ยวทั้ง 4 ด้านรอบสัญลักษณ์ธาตุ แล้วจึงเติมจุดให้เป็นคู่
สัญลักษณ์แบบจุดของลิวอิส
ธาตุต่างๆส่วนใหญ่ไม่เสถียรในรูปอะตอมเดี่ยวยกเว้นธาตุในหมู่ VIIIA (หมู่ 18) หรือเรียกว่าแก๊สมีสกุลที่พบอยู่ในรูปอะตอมเดี่ยว ซึ่งมีจำนวนเวเลนซ์อิเล็กตรอนเท่ากับ 8 ยกเว้นฮีเลียมซึ่งมี 2 เวเลนซ์อิเล็กตรอน
นอกจากนี้นักเคมียังพบว่า อะตอมของธาตุอื่นๆมีแนวโน้มที่จะรวมตัวกันเพื่อที่จะทำให้แต่ละอะตอมมีเวเลนซ์อิเล็กตรอนเท่ากับ 8 จึงมีการสรุปเป็นหลักการที่เรียกว่า กฎออกเตต (octet rule)
สารที่ไม่อยู่ในรูปอะตอมเดี่ยว มีพันธะเคมีระหว่างอะตอมหรือไอออน โดยที่อะตอมของธาตุอาจมีการให้อิเล็กตรอน รับอิเล็กตรอน หรือใช้อิเล็กตรอนร่วมกัน ทำให้เกิดพันธะเคมี 3 ได้แก่ พันธะไอออนิกพันธะโคเวเลนต์ และพันธะโลหะ
3.2 พันธะไอออนิก
สารที่เกิดจากธาตุโลหะกับธาตุอโลหะ มีสมบัติบางประการคล้ายกัน และสารเหล่านี้มีการยึดเหนี่ยวระหว่างอนุภาคที่เหมือนกัน
3.2.1 การเกิดพันธะไอออนิก
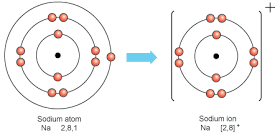
ธาตุโลหะมีพลังงานไอออไนเซชันต่ำจึงเสียอิเล็กตรอนเกิดเป็นไอออนบวกได้ง่ายส่วนธาตุอโลหะมีค่าสัมพรรคภาพอิเล็กตรอนสูง จึงรับอิเล็กตรอนเกิดเป็นไอออนลบ ไอออนบวกและไอออนลบมีประจุไฟฟ้าต่างกันจึงยึดเหนี่ยวกันด้วยแรงดึงดูดระหว่างประจุไฟฟ้า เรียกการยึดเหนี่ยวนี้ว่าพันธะไอออนิกและสารที่เกิดขึ้นจากพันธะไอออนิกว่าสารประกอบไอออนิกชื่อสารประกอบไอออนิกที่เกิดขึ้นส่วนใหญ่เป็นไปตามกฎออกเตตดังตัวอย่าง
สารประกอบไอออนิกในสถานะของแข็งอยู่ในรูปของผลึกที่มีไอออนบวกและไอออนลบยึดเหนี่ยวกันด้วยพันธะไอออนิกอย่างต่อเนื่องกันไปทั้ง 3 มิติเป็นโครงผลึก และไม่อยู่ในรูปโมเลกุล
3.2.2 สูตรเคมีและชื่อของสารประกอบไอออนิก
เราทราบแล้วว่าสารประกอบไอออนิกประกอบด้วยไอออนบวกกับไอออนลบยึดเหนี่ยวกันด้วยแรงดึงดูดระหว่างประจุไฟฟ้า ในการเขียนสูตรสารประกอบไอออนิกจึงต้องทราบว่าแต่ละธาตุที่ทำปฏิกิริยากันนั้นจะเกิดเป็นไอออนชนิดใด และมีจำนวนประจุเท่าใด ซึ่งพิจารณาได้จากการจัดอิเล็กตรอนของธาตุ
สารประกอบไอออนิกเกิดจากไอออนบวกและไอออนลบดังนั้นการเรียกชื่อสารประกอบไอออนิกจึงจำเป็นต้องสร้างชื่อของไอออนบวกและไอออนลบโดยชื่อของไอออนบวกเรียกตามชื่อถ้าเราลงท้ายด้วยคำว่าไอออนส่วนไอออนลบเรียกตามชื่อธาตุโดยเปลี่ยนท้ายเสียงเป็น i-de
จากตารางจะเห็นว่าชื่อไอออนลบของธาตุไฮโดรเจนออกซิเจนและไนโตรเจนมีการตัดคำว่าเช่นออกก่อนจะเปลี่ยนท้ายเป็นเสียง i-de ไอออนที่เป็นกลุ่มอะตอมมีชื่อเรียกเฉพาะโดยกลุ่มอะตอมที่เป็นไอออนบวกลงท้ายด้วย -ium ส่วนกลุ่มอะตอมที่เป็นไอออนลบอาจจะลงท้ายด้วยเสียง -ide -ite -ate
ชื่อสารประกอบไอออนิกได้จากการเรียกชื่อไอออนบวกแล้วตามด้วยชื่อไอออนลบโดยตัดคำว่าไอออนออก ดังตาราง
3.2.3 พลังงานกับการเกิดสารประกอบไอออนิก
การเกิดปฏิกิริยาเคมีจะมีการเปลี่ยนแปลงพลังงานเกิดขึ้นด้วย นักเรียนคิดว่าเมื่อโลหะโซเดียมทำปฏิกิริยากับแก๊สคลอรีนเกิดเป็นโซเดียมคลอไรด์จะเกิดการเปลี่ยนแปลงพลังงานอย่างไร
การศึกษาการเปลี่ยนแปลงพลังงานในการเกิดสารประกอบไอออนิก วิธีการหนึ่งอาจพิจารณาจากวัฎจักรบอร์น-ฮาร์เบอร์ ซึ่งพัฒนาโดยแมกซ์ บอร์น และฟริตซ์ฮาเบอร์ โดยการตั้งสมมติฐานว่าการเกิดสารประกอบไอออนิกชนิดหนึ่งๆ มีหลายขั้น ในแต่ละขั้นจะมีการเปลี่ยนแปลงพลังงานเกิดขึ้นด้วย เราจะพิจารณาการเกิดโซเดียมคลอไรด์จากปฏิกิริยาระหว่างโลหะโซเดียมกับแก๊สคลอรีน ซึ่งมีขั้นตอนต่างๆ ดังนี้
1. การระเหิดของโซเดียม โลหะโซเดียมสถานะของแข็งระเหิดกลายเป็นอะตอมในสถานะแก๊ส ใช้พลังงาน 107 กิโลจูลต่อโมลของโซเดียมอะตอม เรียกพลังงานในขั้นนี้ว่า พลังงานการระเหิด
2. การสลายพันธะของแก๊สคลอรีน โมเลกุลของแก๊สใช้พลังงาน 122 กิโลจูลต่อโมลอะตอมของคลอรีน เรียกพลังงานในขั้นนี้ว่า พลังงานการสลายพันธะ
3. การแตกตัวเป็นไอออนของโซเดียม อะตอมของโซเดียมในสถานะแก๊สเสียอิเล็กตรอนออกไปกลายเป็น ใช้พลังงาน 496 กิโลจูลต่อโมลอะตอมของโซเดียม เรียกพลังงานในขั้นนี้ว่า พลังงานไอออไนเซชัน
4. การเกิดคลอไรด์ไอออน อะตอมของคลอรีนในสถานะแก๊สรับอิเล็กตรอนที่หลุดออกจากอะตอมของโซเดียมกลายเป็น คายพลังงาน 349 กิโลจูลต่อโมลของคลอไรด์ไอออน พลังงานในขั้นนี้เรียกว่า สัมพรรคภาพอิเล็กตรอน
5. การเกิดโซเดียมคลอไรด์ โซเดียมไอออนกับคลอไรด์ไอออนในสถานะแก๊สรวมตัวกันเป็นผลึกโซเดียมคลอไรด์และคายพลังงานออกมา 787 กิโลจูลต่อโมลของโซเดียมคลอไรด์ เรียกพลังงานในขั้นนี้ว่า พลังงานโครงผลึกหรือพลังงานแลตทิซ
3.2.4 สมบัติของสารประกอบไอออนิก
สารประกอบไอออนิกประกอบด้วยไอออนบวกกับไอออนลบ เมื่อทุบผลึกของสารไอออนิกจะเกิดการเลื่อนไถลของไอออนไปตามระนาบผลึก เป็นผลให้ไอออนชนิดเดียวกันเลื่อนไปอยู่ตรงกัน จึงเกิดแรงผลักระหว่างไอออน ทำให้ผลึกแตกออก ดังรูป 2.5 เราจึงสังเกตพบว่าสารไอออนิกเปราะและแตกได้ง่าย
สภาพละลายได้ของสาร เป็นความสามารถของสารที่จะละลายในสารอื่นจนเป็นสารละลายอิ่มตัวสภาพละลายได้ส่วนใหญ่หมายถึงการละลายของสารในน้ำ
* การบอกสภาพละลายได้โดยทั่วไปมี 3 ระดับคือ
- ละลายได้ดี หมายถึงละลายได้มากกว่า 1 กรัมในน้ำ 100 กรัม
- ละลายได้เล็กน้อยหรือละลายได้บางส่วน หมายถึงละลายได้มากกว่า 0.1 กรัม แต่ไม่เกิน 1กรัมในน้ำ 100 กรัม
- ไม่ละลาย หมายถึงละลายได้น้อยกว่า 0.1 กรัมในน้ำ 100 กรัม
การละลายของสารเป็นการกระจายของตัวละลายเข้าไปอยู่ระหว่างอนุภาคของตัวทำละลาย ขณะที่สารเกิดการละลาย แรงยึดเหนี่ยวระหว่างอนุภาคในตัวละลายและตัวทำละลายจะถูกทำลาย ในขณะเดียวกันก็มีการสร้างแรงยึดเหนี่ยวระหว่างอนุภาคของตัวทำละลายกับอนุภาคของตัวละลาย
พลังงานแลตทิซ คือพลังงานที่คายออกเมื่อไอออนบวกกับไอออนลบในสถานะแก๊สรวมตัวกันเกิดเป็นโครงผลึกส่วนการทำให้ไอออนบวกและไอออนลบในโครงผลึกหลุดออกมาเป็นกระบวนการย้อนกลับ จึงต้องใช้พลังงานเท่ากับพลังงานแลตทิซ
3.3 พันธะโคเวเลนต์
สารที่เกิดจากธาตุอโลหะรวมตัวกันเช่นแก๊สออกซิเจนแก๊สไนโตรเจนและแก๊สคาร์บอนไดออกไซด์ การยึดเหนี่ยวระหว่างอะตอมของธาตุในสารเหล่านี้เป็นพันธะไอออนิกหรือไม่เพราะเหตุใด
3.3.1 การเกิดพันธะโคเวเลนต์
ธาตุอโลหะมีค่าอิเล็กโทรเนกาติวิตีสูงดังนั้นเมื่อรวมตัวกันจะไม่มีอะตอมใดยอมเสียอิเล็กตรอน อะตอมจึงยึดเหนี่ยวกันโดยใช้เวเลนซ์เล็กตรอนร่วมกันเรียกการยึดเหนี่ยวในว่าพันธะโคเวเลนต์แล้วนะสารที่อะตอมยึดเหนี่ยวกันด้วยพันธะโคเวเลนต์ว่าสารโคเวเลนต์ซึ่งส่วนใหญ่อยู่ในรูปโมเลกุลโดยการเกิดพันธะในโมเลกุลโคเวเลนต์ส่วนใหญ่เป็นไปตามกฎออกเตตดังตัวอย่าง
คลอรีนมีเวเลนซ์อิเล็กตรอนเท่ากับ 7 ดังนั้นข้อดีทั้ง 2 อะตอมจะใช้เวลาดิจิตอลร่วมกัน 1 คู่เพื่อให้มีเวเลนซ์อิเล็กตรอนครบ 8 ตามกฎออกเตต เขียนแผนภาพและสัญลักษณ์แบบจุดของลิวอิสแสดงการเกิดพันธะได้ดังนี้
พันธะโคเวเลนต์ในโมเลกุลแก๊สคลอรีนเกิดจากการใช้เวเลนซ์อิเล็กตรอนร่วมกัน 1 คู่พันธะนี้เรียกว่าพันธะเดี่ยว ด้วยอิเล็กตรอนคู่ที่ใช้ร่วมกันในการเกิดพันธะเรียกว่าอิเล็กตรอนคู่ร่วมพันธะส่วนอิเล็กตรอนคู่ที่ไม่ได้เกิดพันธะเรียกว่าอิเล็กตรอนคู่โดดเดี่ยวซึ่งในโมเลกุลแก๊สคลอรีนมีอิเล็กตรอนคู่ร่วมพันธะ 1 คู่และมีอิเล็กตรอนคู่โดดเดี่ยว 6 คู่
อีกทั้งยังมีการเกิดพันธะในโมเลกุล ออกซิเจนแต่ละอะตอมมีเวเลนซ์อิเล็กตรอนเท่ากับ 6 ดังนั้นออกซิเจนทั้ง 2 อะตอมจะใช้เวทีเล็กตอนร่วมกัน 2 คู่เพื่อให้เป็นไปตามกฎออกเตต เกิดพันธะโคเวเลนต์แบบพันธะคู่ นอกจากนี้พันธะโคเวเลนต์ยังอาจเป็นพันธะสาม เช่นในโมเลกุลแก๊สไนโตรเจนไนโตรเจนแต่ละอะตอมมีเวเลนซ์อิเล็กตรอนเท่ากับ 5 ดังนั้นไนโตรเจนทั้ง 2 อะตอมจะใช้เวลาที่เล็กตอนร่วมกัน 3 คู่เพื่อให้เป็นไปตามกฎออกเตต
3.3.2 การเขียนสูตรและเรียกชื่อสารโคเวเลนต์
สูตรโมเลกุลของสารโคเวเลนต์โดยทั่วไปเขียนสัญลักษณ์ของธาตุองค์ประกอบโดยเรียงลำดับจากค่าอิเล็กโทรเนกาติวิตีน้อยไปมากพร้อมทั้งระบุจำนวนอะตอมของธาตุที่มีจำนวนอะตอมมากกว่า 1 อะตอมยกเว้นสามารถชนิดเช่น NH3 และ CH4 ทั้งที่ถ้าไนโตรเจนและธาตุคาร์บอนมีอิเล็กโทรเนกาติวิตีสูงกว่าธาตุไฮโดรเจน
การเรียกชื่อสารโคเวเลนต์มีหลักการดังนี้
1.สารโคเวเลนต์ที่ประกอบด้วยธาตุชนิดเดียวกันเรียกตามชื่อท่านนั้นซึ่งท่านเหล่านี้ส่วนใหญ่มีสถานะเป็นแก๊สที่อุณหภูมิห้องจึงนิยมเรียกชื่อโดยระบุสถานะด้วยเพื่อให้ทราบว่าเป็นการกล่าวถึงโมเลกุลที่ไม่ใช่อะตอมของธาตุเช่นแก๊สออกซิเจน
2.สารโคเวเลนต์ที่ประกอบด้วยธาตุ 2 ชนิดให้เรียกชื่อธาตุตามลำดับที่ปรากฏในสูตรโมเลกุลโดยเปลี่ยนพยางค์ท้ายเป็น -ide และระบุจำนวนอะตอมองค์ประกอบ ในโมเลกุลด้วยคำภาษากรีก ดังตาราง
ตัวอย่างการเขียนสูตรและการเรียกชื่อสารประกอบโคเวเลนต์
3.3.3 ความยาวพันธะและพลังงานพันธะของสารโคเวเลนต์
จากกราฟในรูป การเกิดโมเลกุลของแก๊สไฮโดรเจนนั้น อะตอมของไฮโดรเจนจะเคลื่อนที่เข้าใกล้กันได้มากที่สุดและเกิดสมดุลระหว่างแรงดึงดูดกับแรงผลักที่ระยะ 74 พิโกเมตร ถ้าเข้าใกล้กันมากกว่านี้ แรงผลักจะเพิ่มมากขึ้นและโมเลกุลจะไม่เสถียร ระยะ 74 พิโกเมตรจึงเป็นระยะที่สั้นที่สุดที่นิวเคลียสของอะตอมทั้งสองสร้างพันธะกันในโมเลกุล ระยะนี้เรียกว่า ความยาวพันธะ ความยาวพันธะหาได้จากการศึกษาการเลี้ยวเบนรังสีเอกซ์ (X - ray diffraction) ผ่านโครงผลึกของสารหรือจากการศึกษาวิเคราะห์สเปกตรัมของโมเลกุลของสาร
เมื่อพิจารณาข้อมูลในตารางจะพบว่าความยาวพันธะระหว่างอะตอม O กับ H ในโมเลกุลของสารต่างชนิดกันมีค่าแตกต่างกันและแตกต่างจากข้อมูลที่สืบค้นได้คือความยาวพันธะ O-H เท่ากับ 97 พิโกเมตร เนื่องจากความยาวพันธะระหว่างอะตอมคู่หนึ่งหาได้จากค่าเฉลี่ยของความยาวพันธะระหว่างอะตอมคู่เดียวกันในโมเลกุลชนิดต่างๆ ดังนั้นเมื่อกล่าวถึงความยาวพันธะ โดยทั่วไปจึงหมายถึง ความยาวพันธะเฉลี่ย
สำหรับความยาวพันธะเฉลี่ยระหว่างอะตอมคู่ต่างๆแสดงดังตาราง
จากตาราง จะเห็นว่าพันธะระหว่างคาร์บอนมีทั้งพันธะเดี่ยวพันธะคู่และพันธะสามซึ่งมีค่าพลังงานพันธะเป็น 346 614 และ 839 กิโลจูลต่อโมลตามลำดับ แสดงว่าพันธะสามแข็งแรงกว่าพันธะคู่และพันธะคู่แข็งแรงกว่าพันๆเดี่ยวและถ้าพิจารณาอะตอมคู่ร่วมพันธะๆเดียวกันของแท้ที่มีค่าพลังงานน้อยจะมีความยาวพันธะมาก นอกจากอะตอมคู่ร่วมพันธะเดียวกันแล้วความสัมพันธ์นี้ยังสามารถใช้เปรียบเทียบพันธะของธาตุในหมู่เดียวกันได้อีกด้วย
ปฏิกิริยาเคมีที่เกี่ยวข้องกับกระบวนการสลายพันธะในสารตั้งต้นและการสร้างพันธะเกิดเป็นผลิตภัณฑ์โดยการสลายพันธะเป็นกระบวนการดูด (E1) พลังงานซึ่งมีค่าเป็นบวกและการสร้างพันธะจะมีค่าเป็นลบเป็นกระบวนการคายพลังงาน (E2) และพลังงานของปฏิกิริยา (เดลต้า H) คำนวณได้จากผลรวมของ
3.3.4 รูปร่างโมเลกุลโคเวเลนต์
การศึกษาในเรื่องความยาวพันธะทำให้ทราบระยะห่างระหว่างนิวเคลียสของอะตอมที่สร้างพันธะในโมเลกุลแต่ความยาวพันธะไม่สามารถบอกลักษณะการจัดเรียงอะตอมในโมเลกุลแบบสามมิติหรือรูปร่างโมเลกุลได้
เพื่อให้เกิดความเข้าใจเกี่ยวกับรูปร่างโมเลกุลของโมเลกุลที่มีจำนวนอะตอมตั้งแต่ 3 อะตอมขึ้นไป ให้ศึกษาการจัดเรียงตัวของลูกโป่งแล้วนำมาอุปมาอุปไมยกับการจัดเรียงอะตอมในโมเลกุลจากการทดอลงต่อไปนี้ ที่นี่
จากกิจกรรม ในตอนที่ 1 ลูกโป่งแต่ละลูกซึ่งมีปริมาตรเท่ากันเมื่อนำมาผูกข้อติดกันพบว่าลูกโป่งแต่ละรูปผัดกันเกิดการจับตัวเป็นรูปร่างต่างๆที่สมมาตรในที่มีลูกโป่งเป็นตัวแทนของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอะตอมกลางและอะตอมล้อมรอบซึ่งอิเล็กตรอนเหล่านี้จะผลักกันด้วยแรงกระทำระหว่างประจุชนิดเดียวกันทำให้ได้คิดค่าของพันธะอยู่ห่างกันมากที่สุดเกิดเป็นรูปร่างโมเลกุลในลักษณะเดียวกันกับการจัดตัวของลูกโป่ง และในกิจกรรมตอนที่ 2 ลูกโป่งต่างสีใช้แทนอิเล็กตรอนคู่ร่วมพันธะและอิเล็กตรอนคู่โดดเดี่ยวซึ่งรูปร่างโมเลกุลพิจารณาจากตำแหน่งของอะตอมทั้งหมดโดยไม่นำตำแหน่งของอิเล็กตรอนคู่โดดเดี่ยวมาพิจารณา การคาดคะเนรูปร่างโมเลกุลจากโครงสร้างลิวอิสโดยอาศัยการผลักกันของอิเล็กตรอนคู่ร่วมพันธะและอิเล็กตรอนคู่โดดเดี่ยวอาจใช้ทฤษฎีการผลักระหว่างคู่อิเล็กตรอนในวงเวเลนซ์ (VSEPR) โดยทฤษฎีนี้มีหลักการว่าอิเล็กตรอนคู่โดดเดี่ยวอยู่ใกล้นิวเคลียสมากกว่าอิเล็กตรอนคู่ร่วมพันธะดังนั้นรหัสระหว่างอิเล็กตรอนคู่โดดเดี่ยวด้วยกันจึงมีค่ามากกว่าแรงผลักระหว่างอิเล็กตรอนคู่ร่วมพันธะกับอิเล็กตรอนคู่โดดเดี่ยว และมากกว่าแรงผลักระหว่างอิเล็กตรอนคู่ร่วมพันธะด้วยกัน
จากผลการทดลองกิจกรรมการจับตัวของลูกโป่งกับรูปร่างโมเลกุลโคเวเลนต์สรุปรูปร่างโมเลกุลโคเวเลนต์ดังตาราง
3.3.5 สภาพขั้วของโมเลกุลโคเวเลนต์
สารโคเวเลนต์ที่เกิดจากอะตอมชนิดเดียวกันเช่นแก๊สไฮโดรเจนมีการกระจายของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอะตอมทั้งสองเท่ากันทั้งๆที่เกิดขึ้นในลักษณะเช่นนี้จะเรียกว่าพันธะโคเวเลนต์ไม่มีขั้วและสารโคเวเลนต์ที่เกิดจากอะตอมต่างชนิดกันและมีค่าอิเล็กโทรเนกาติวิตีแตกต่างกันจะมีการกระจายของกลุ่มหมอกอิเล็กตรอนคู่ร่วมพันธะระหว่างอะตอมไม่เท่ากันเช่นไฮโดรเจนคลอไรด์มีอิเล็กตรอนคู่ร่วมพันธะอยู่บริเวณอะตอมคลอรีนมากกว่าอะตอมไฮโดรเจนเพราะอะตอมคลอรีนมีค่าอิเล็กโทรเนกาติวิตีมากกว่าอะตอมไฮโดรเจนทำให้อะตอมของดีแสดงประจุไฟฟ้าค่อนข้างรถยนต์อะตอมไฮโดรเจนมีค่าอิเล็กโทรเนกาติวิตีน้อยกว่าแสดงประจุไฟฟ้าค่อนข้างบวก ที่เกิดขึ้นลักษณะนี้เรียกว่าพันธะโคเวเลนต์มีขั้ว การแสดงขั้วของพันธะอาจใช้สัญลักษณ์ เดลต้าบวก สำหรับอะตอมที่แสดงประจุไฟฟ้าค่อนข้างบวก และเดลต้าลบ สำหรับอะตอมที่แสดงประจุไฟฟ้าค่อนข้างลบหรืออาจใช้เครื่องหมายโดยให้หัวลูกศรหันชี้ไปในทิศของอะตอมที่แสดงประจุไฟฟ้าค่อนข้างลบส่วนท้ายลูกศร ที่มีลักษณะคล้ายเครื่องหมายบวกให้อยู่บริเวณอะตอมที่แสดงประจุไฟฟ้าค่อนข้างบวก
ของพันธะทำให้โมเลกุลอะตอมคู่ที่ประกอบด้วยธาตุชนิดเดียวกันเป็นโมเลกุลไม่มีขั้วโมเลกุลอะตอมคู่ที่ประกอบด้วยธาตุต่างชนิดกันเป็นโมเลกุลมีขั้วและโมเลกุลโคเวเลนต์ที่ประกอบด้วยอะตอมมากกว่า 2 อะตอม และพันธะระหว่างครูอะตอมเป็นพันธะมีขั้วจะเป็นโมเลกุลมีขั้วหรือไม่อย่างไร สภาพขั้วของโมเลกุลที่ประกอบด้วยอะตอมมากกว่า 2 อะตอมพิจารณาจากการรวมสภาพขั้วของพันธะแบบเวกเตอร์ ซึ่งถ้าเวกเตอร์ หักหลังกันหมดจะทำให้โมเลกุลไม่มีขั้วแต่ถ้าเวกเตอร์แทนละกันไม่หมดโมเลกุลจะเป็นโมเลกุลที่มีขั้ว
โมเลกุลที่อะตอมกลางไม่มีอิเล็กตรอนคู่โดดเดี่ยว และอะตอมล้อมรอบเหมือนกันทุกอะตอมเป็นโมเลกุลไม่มีขั้วถึงแม้ว่าพันธะภายในโมเลกุลจะเป็นพันธะที่มีขั้วแต่เนื่องจากรูปร่างโมเลกุล
สำหรับโมเลกุลที่อะตอมกลางมีอิเล็กตรอนคู่โดดเดี่ยวหรือมีอะตอมล้อมรอบเป็นธาตุต่างชนิดกันส่วนใหญ่เป็นโมเลกุลมีขั้วเนื่องจากเวกเตอร์สภาพขั้วของพันธะหักล้างกันไม่หมด
โมเลกุลอะตอมกลางมีอิเล็กตรอนคู่โดดเดี่ยวส่วนใหญ่เป็นโมเลกุลแบบมีขั้วและมีบางชนิดอาจเป็นโมเลกุลไม่มีขั้วเนื่องจากมีรูปร่างโมเลกุลแบบสี่เหลี่ยมแบนราบทำให้เวกเตอร์สภาพขั้วหักล้างกันหมดโมเลกุลอะตอมกลางมีอิเล็กตรอนคู่โดดเดี่ยวส่วนใหญ่เป็นโมเลกุลแบบมีขั้วและมีบางชนิดอาจเป็นโมเลกุลไม่มีขั้วเนื่องจากมีรูปร่างโมเลกุลแบบสี่เหลี่ยมแบนราบทำให้เวกเตอร์สภาพขั้วหักล้างกันหมด
3.3.6 แรงยึดเหนี่ยวระหว่างโมเลกุลและสมบัติของสารโคเวเลนต์
ที่อุณหภูมิห้องสารโคเวเลนต์แต่ละชนิดอันอยู่ในสถานะที่แตกต่างกันทั้งนี้ขึ้นอยู่กับแรงยึดเหนี่ยวระหว่างโมเลกุลหรือแรงแวนเดอร์วาลส์ โดยในสถานะของแข็งโมเลกุลอยู่ชิดกันจนไม่สามารถเคลื่อนที่ได้และมีแรงยึดเหนี่ยวระหว่างโมเลกุลมากในสถานะของเหลวโมเลกุลสามารถเคลื่อนที่ได้แต่ยังคงอยู่ชิดติดกันและมีแรงยึดเหนี่ยวระหว่างโมเลกุลน้อยกว่าในของแข็งส่วนในสถานะแก๊สโมเลกุลอยู่ห่างกันสามารถเคลื่อนที่ได้อย่างอิสระและมีแรงยึดเหนี่ยวระหว่างโมเลกุลน้อยมากจนถือว่าไม่มีแรงยึดเหนี่ยวระหว่างโมเลกุลดังนั้นการเปลี่ยนแปลงสถานะของสารจากของแข็งไปเป็นของเหลว หรือของเหลวไปเป็นแก๊สซึ่งเกี่ยวข้องกับการทำลายงานยึดเหนี่ยวระหว่างโมเลกุลโดยไม่มีการทำลายพันธะโคเวเลนต์ ซึ่งแรงยึดเหนี่ยวระหว่างโมเลกุลมีค่าพลังงานน้อยกว่าพันธะโคเวเลนต์มากสามารถทำลายได้ด้วยการให้พลังงานความร้อนแก้สารจนกระทั่งโมเลกุลของสารมีพลังงานจลน์สูงพอที่จะเกิดการเปลี่ยนแปลงสถานะได้ดังนั้นสารแต่ละชนิดซึ่งมีแรงยึดเหนี่ยวระหว่างโมเลกุลที่แตกต่างกันจะมีจุดหลอมเหลวและจุดเดือดที่ต่างกันด้วย
นอกจากจุดหลอมเหลวของสารที่จะเกี่ยวข้องกับแรงยึดเหนี่ยวระหว่างโมเลกุลแล้วยังขึ้นอยู่กับการจัดเรียงโมเลกุลในของแข็งทำให้แนวโน้มของจุดหลอมเหลวอาจไม่สอดคล้องกับแรงยึดเหนี่ยวระหว่างโมเลกุลโดยตรง
แรงยึดเหนี่ยวระหว่างโมเลกุลเกี่ยวข้องกับขนาดของโมเลกุลและสภาพขั้วของโมเลกุลซึ่งแรงยึดเหนี่ยวระหว่างโมเลกุลมีหลายชนิดและมีชื่อเรียกที่ต่างกันซึ่งในที่นี้จะกล่าวถึง 3 ชนิดที่สำคัญดังนี้
1.และแพร่กระจายลอนดอน แรงแพร่กระจายลอนดอน เป็นแรงยึดเหนี่ยวระหว่างโมเลกุลไม่มีขั้วหรืออะตอมแก๊สมีสกุลซึ่งเป็นแรงอย่างอ่อนๆที่เกิดขึ้นจากการกระจายของอิเล็กตรอนในอะตอมขณะใดขณะหนึ่งซึ่งอาจไม่เท่ากันจึงทำให้สภาพขั้วชั่วขณะ แล้วเหนี่ยวนำให้โมเลกุลที่อยู่ติดกันเกิดขั้วตรงข้ามและมีแรงดึงดูดชั่วขณะ โดยแรงแผ่กระจายนี้เพิ่มขึ้นตามขนาดของโมเลกุลเนื่องจากโมเลกุลขนาดใหญ่สามารถเกิดสภาพขั้วชั่วขณะได้มากกว่า
2.แรงระหว่างขั้วสำหรับโมเลกุลมีขั้วนอกจากจะมีแรงแผ่กระจายลอนดอนแล้ว ยังมีแรงดึงดูดที่เกิดจากสภาพของขั้วโมเลกุลด้วยโมเลกุลที่อยู่ใกล้กันจะหันส่วนของโมเลกุลที่มีขั้วตรงข้ามกันเข้าหากันเกิดเป็นแรงดึงดูดทางไฟฟ้าจากสภาพขั้วนี้โดยทั่วไปในระหว่างขั้วเพิ่มขึ้นตามสภาพขั้วของโมเลกุลที่มีขนาดใกล้เคียงกัน
3.พันธะไฮโดรเจนเมื่อพิจารณาจุดเดือดของสารประกอบไฮโดรเจนกับธาตุหมู่ VIIA จะเห็นว่า HF มีจุดเดือดสูงกว่าสารประกอบอื่นทั้งที่มีขนาดโมเลกุลเล็กที่สุดซึ่งไม่เป็นไปตามแนวโน้มของขนาดโมเลกุลดังที่ได้กล่าวมาแล้วข้างต้นแสดงว่า HF มีแรงดึงดูดระหว่างโมเลกุลมากกว่าสารประกอบของไฮโดรเจนกับธาตุหมู่ VIIA อื่นๆ ทั้งนี้เพราะผลต่างของค่าอิเล็กโทรเนกาติวิตีระหว่างไฮโดรเจนกับฟลูออรีนมีค่ามากทำให้กลุ่มหมอกอิเล็กตรอนอยู่ทางด้านอะตอมฟลูออรีนที่มีขนาดเล็กอย่างหนาแน่นอะตอมฟลูออรีนและไฮโดรเจนมีสภาพขั้วสูงกว่าในกรณีที่ HCl HBr และ HI มาก ทำให้มีแรงดึงดูดระหว่างโมเลกุลมากด้วยแรงดึงดูดระหว่างโมเลกุลที่เกิดขึ้นจากอะตอมไฮโดรเจนของโมเลกุลหนึ่งกับอิเล็กตรอนคู่โดดเดี่ยวบนอะตอมของธาตุที่มีขนาดเล็กและมีอิเล็กโทรเนกาติวิตีสูงของอีโมเลกุลหนึ่งเรียกแรงดึงดูดนี้ว่า พันธะไฮโดรเจน
3.4 พันธะโลหะ
โลหะบางชนิดเส้นทองแดง เหล็กอะลูมิเนียมมีสมบัติบางประการคล้ายกับแสดงว่าสารเหล่านี้มีการยึดเหนี่ยวกันระหว่างอนุภาคที่เหมือนกันและอะตอมธาตุโลหะสร้างพันธะเคมีระหว่างกันอย่างไรเหมือนหรือต่างกัน จากพันธะไอออนิกและโคเวเลนต์หรือไม่
3.4.1 การเกิดพันธะโลหะ
จากที่ทราบแล้วว่าโลหะส่วนใหญ่มีสถานะเป็นของแข็งมีจุดหลอมเหลวและจุดเดือดสูงผิวมันวาวสามารถนำไฟฟ้าและความร้อนได้ดีจะสมบัติดังกล่าวจะเห็นว่าโลหะมีสมบัติบางประการของสารประกอบไอออนิกและมีสมบัติบางประการที่แตกต่างจากสารประกอบไอออนิกเช่นการนำไฟฟ้าและการนำความร้อนได้ดีในสถานะของแข็งผิวมันวาวและสมบัติส่วนใหญ่ต่างจากพันธะโคเวเลนต์ซึ่งแสดงว่าโลหะน่าจะยึดเหนี่ยวกันด้วยพันธะที่แตกต่างจากพันธะไอออนิกและพันธะโคเวเลนต์การที่อะตอมของโลหะมีค่าพลังงานไอออไนเซชันต่างการยึดเหนี่ยวระหว่างวาเลนอิเล็กตรอนกับโปรตอนในนิวเคลียสจึงน้อยให้เวเลนซ์อิเล็กตรอนของแต่ละอะตอมสามารถเคลื่อนที่ได้อย่างอิสระไปทั่วทั้งชิ้นโลหะและเกิดการยึดเหนี่ยวกับโปรตอนในนิวเคลียสทุกทิศทุกทางการยึดเหนี่ยวนี้เรียกว่าพันธะโลหะการเกิดพันธะโลหะแสดงได้ด้วยแบบจำลองทะเลอิเล็กตรอน
3.4.2 สมบัติของโลหะ
1.โลหะมีจุดหลอมเหลวและจุดเดือดสูง
2.โลหะมีผิวมันวาวและสามารถสะท้อนแสงได้
3.โลหะนำไฟฟ้าและความร้อนได้ดี นอกจากนี้โลหะยังสามารถตีให้ออกเป็นแผ่นและดึงให้
3.5 การใช้ประโยชน์ของสารประกอบไอออนิก สารโคเวเลนต์ และโลหะ
จากการที่สารประกอบไอออนิกสารโคเวเลนต์และโลหะมีสมบัติเฉพาะตัวมาว่าการที่ต่างกันจึงสามารถนำมาใช้ประโยชน์ในด้านต่างๆได้ตามความเหมาะสม เช่น
- แอมโมเนียมคลอไรด์และซิงค์คลอไรด์ เป็นสารประกอบไอออนิกที่สามารถนำไฟฟ้าได้จากการแตกตัวเป็นไอออนเมื่อละลายน้ำจึงนำไปใช้เป็นสารอิเล็กโทรไลต์ในถ่านไฟฉาย
- พอลิไวนิลคลอไรด์หรือ PVC เป็นสารโคเวเลนต์ที่ไม่สามารถนำไฟฟ้าได้จึงเป็นฉนวนไฟฟ้าที่หุ้มสายไฟฟ้า
- ซิลิกอนคาร์ไบด์ เป็นสารโคเวเลนต์โครงร่างตาข่ายที่มีจุดหลอมเหลวสูงและมีความแข็งแรงมากจึงนำไปใช้ทำเครื่องบด
- ทองแดงและอะลูมิเนียม เป็นโลหะที่นําไฟฟ้าได้ดีจึงนำไปใช้เป็นตัวนำไฟฟ้าอลูมิเนียมและเหล็กเป็นโลหะที่นําความร้อนได้ดีจึงนำไปทำภาชนะสำหรับประกอบอาหาร เช่น หม้อ กะทะ



























ไม่มีความคิดเห็น:
แสดงความคิดเห็น